一、研究背景
DNA损伤是细胞生命周期中持续发生的分子事件。环境因素(如紫外线、化学毒物)及细胞内正常的代谢过程(如氧化呼吸链产生的活性氧)均可导致DNA结构改变。据统计,每个细胞每天约发生1000至100万次分子损伤事件。尽管这一数字相对于人类基因组约60亿个碱基(30亿个碱基对)的总量而言占比甚微,但若关键基因上的损伤未能得到及时修复,将直接影响细胞的正常功能,并显著增加癌变风险。
彗星检测,又称单细胞凝胶电泳,是目前评估单个细胞DNA损伤的常用技术。其基本原理为:在电场作用下,含有碎片和链断裂的受损DNA迁移速度高于完整DNA,从而在显微镜下呈现经典的“彗星拖尾”形态。研究人员通常通过测量彗尾长度来半定量评估DNA损伤程度,也可借助图像分析软件对尾矩、尾部DNA百分比等多个参数进行精确分析。
二、产品特性与应用场景
由艾美捷代理Cell Biolabs公司推出的OxiSelect 24孔彗星检测专用玻片(货号:STA-836),是专为彗星检测实验设计的表面处理型玻片。该玻片经过特殊的化学修饰,能够有效粘附彗星检测中常用的低熔点琼脂糖,确保在裂解、电泳等操作步骤中凝胶层不易脱落,从而提高实验的稳定性和可重复性。
该产品具有以下技术特点:
孔板规格:24孔设计,支持多样本平行处理,便于进行剂量效应实验、时间梯度实验或不同细胞类型的比较研究。
兼容性强:既可与OxiSelect 24孔彗星检测试剂盒(货号STA835)中的配套试剂联合使用,也支持用户自备的彗星检测试剂体系。这为已有成熟实验方案的研究人员提供了灵活选择。
操作便利:玻片直接适配标准电泳槽和离心转子,无需自行准备载玻片、包被处理或密封边缘,显著简化实验流程。
典型应用场景包括:
药物或环境污染物对细胞DNA损伤程度的筛选与评价
DNA修复机制研究(结合不同时间点的损伤动力学分析)
抗氧化剂或保护剂的功效评估
肿瘤细胞对化疗药物敏感性的检测
三、操作流程要点
使用该玻片进行彗星检测时,推荐流程如下:
1.包埋细胞:将待测细胞悬液与熔融的低熔点琼脂糖混合,迅速滴加至玻片的各孔中,4℃凝固。
2.裂解:加入裂解液(含高浓度盐和去垢剂)去除细胞膜和可溶性蛋白,暴露核DNA。
3.解旋:碱性条件下(pH > 13)使DNA双链解旋,断裂位点转化为单链缺口。
4.电泳:在水平电泳槽中进行碱性电泳,受损DNA片段迁移出核区形成彗尾。
5.中和、染色与观察:中和玻片后,使用DNA荧光染料(如Vista Green)染色,在荧光显微镜下采集图像并分析。
用户若自备试剂,需确保裂解液、电泳缓冲液和染料的配制符合碱性彗星检测的标准要求。
四、典型结果示例
以下展示使用该玻片获得的代表性实验结果,数据仅供技术参考,不宜直接用于解释实际检测结果。
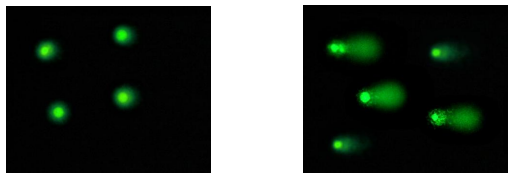

图1. 依托泊苷对Jurkat细胞的处理。在进行彗星实验(碱性电泳条件,33 V/300 mA,持续15分钟)前,Jurkat细胞未处理(左)或用20 ?M依托泊苷处理(右)4小时。
Jurkat细胞(人T细胞白血病细胞系)分为两组:
未处理组(图左):细胞核呈圆形或椭圆形,荧光均匀,无明显的彗尾拖尾现象,表明DNA保持完整。
处理组(图右):加入20 ?M依托泊苷(一种拓扑异构酶II抑制剂,可诱导DNA链断裂)处理4小时后,在相同电泳条件下(碱性电泳,33 V,300 mA,15分钟),细胞核出现明显的彗星状拖尾,彗尾长度和尾部荧光强度显著增加,表明DNA发生了大量链断裂。
该结果验证了该玻片能够清晰区分不同DNA损伤程度的细胞样本,且背景低、孔间重复性良好。
五、注意事项
1. 玻片为一次性使用耗材,不可重复利用,以免表面化学处理层失效。
2. 低熔点琼脂糖的加热温度不宜过高(通常加热至约70℃溶解后冷却至37℃左右与细胞混合),以免造成细胞热损伤。
3. 电泳条件(电压、电流、时间)需根据细胞类型和损伤程度进行预实验优化。
4. 染色后应尽快在荧光显微镜下观察和拍照,避免荧光淬灭。
文献参考:
1. Ostling, O., and Johanson, K. J. (1984). Micro gel electrophoretic study of radiation induced DNA
damages in individual mammalian cells. Biochem. Biophys. Res. Commun. 123, 291–298.
2. Singh, N. P., McCoy, M. T., Tice, R. R., and Schneider, E. L. (1988). A simple technique for
quantification of low levels of DNA damage in individual cells. Exp. Cell. Res. 175, 184–191.
3. Olive, P. L., Banath, J. P., and Durand, R. E. (1990a). Heterogeneity in radiation induced DNA
damage and repair in tumor and normal cells using the "Comet" assay. Radiat. Res. 122, 86–94.
4. De Boeck, M., Touil, N., De Visscher, G., Vande, P. A., and KirschVolders, M. (2000). Validation
and implementation of an internal standard in Comet assay. Mutat. Res. 469, 181–197.

微信扫码在线客服