氯膦酸二钠,化学名称为二氯亚甲基二膦酸二钠,隶属于双膦酸盐家族,为第一代双膦酸盐药物。其在临床应用中占据重要地位,常作为一线治疗药物,广泛应用于恶性肿瘤并发的高钙血症、溶骨性癌转移所引发的骨痛,同时能够有效避免或延缓恶性肿瘤的溶骨性骨转移,以及治疗多种类型的骨质疏松。该药物既有口服的胶囊剂型,也有适用于静脉滴注的注射液剂型。
作为骨代谢的重要调节剂,氯膦酸二钠能够深入骨基质羟磷灰石晶体内部。当破骨细胞对晶体进行吸收时,药物随之释放,进而有效抑制破骨细胞的活性,并通过成骨细胞间接发挥抑制骨吸收的作用。
Clodronate作为一种不含氮的二膦酸盐,与含氮亚类通过截然不同的生化机制(即甲羟戊酸途径)对破骨细胞及其他细胞产生影响。不含氮的二膦酸盐,如氯膦酸盐,在细胞内被代谢为不可水解的ATP类似物。这一过程通过抑制线粒体中的ADP/ATP转运机制,进而诱导细胞发生凋亡。
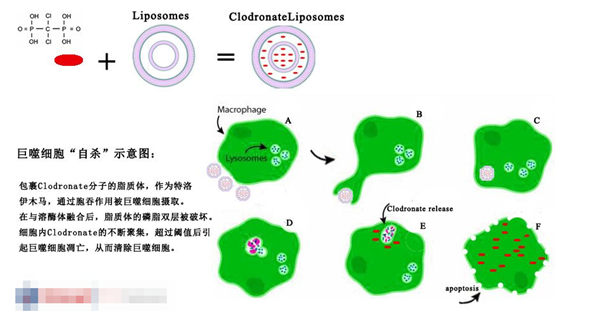
值得注意的是,Clodronate本身并不具有毒性,且其脂质体(若由磷脂酰胆碱和胆固醇组成)同样无毒。游离状态的氯膦酸盐难以穿透脂质体和细胞膜的磷脂双层结构,但脂质体却易于被巨噬细胞吞噬。这意味着,当氯膦酸盐以脂质体为载体被递送到吞噬细胞中后,它将无法从细胞中逃逸。在巨噬细胞内溶酶体磷脂酶的作用下,脂质体的双层结构遭到破坏,溶解在脂质体双层之间水性区室中的药物随即被释放到细胞中。随着氯膦酸盐在细胞内的不断积累,当其浓度超过一定阈值时,细胞将受到不可逆的损伤,并最终通过细胞凋亡的方式走向死亡。而游离的氯膦酸盐,例如从死亡的巨噬细胞中释放出来的部分,在循环系统中的半衰期极短,主要通过肾脏系统被清除出体外。
当然,这一方法的有效性前提是脂质体能够成功到达需要被清除的巨噬细胞所在位置。然而,脂质体并无法穿越血管屏障(如毛细血管壁)。简而言之,在脂质体剂量充足的情况下,巨噬细胞可以在肝脏(枯否细胞)、脾脏(红髓)、肺(肺泡但非间质巨噬细胞,间质巨噬细胞的作用尚存争议)、腹膜腔、淋巴结、关节(滑膜衬里细胞)以及睾丸等部位被有效清除。
脂质体作为一种人工制备的脂质囊泡结构,由亲水性隔室的同心磷脂双层所组成。它们能够用于包封溶解在水溶液中的强亲水性分子,如氯膦酸盐这一无毒的二膦酸盐。自由溶解状态的氯膦酸盐无法穿透脂质体或细胞的磷脂膜。在注射后,这些作为“特洛伊木马”的脂质体将被巨噬细胞摄取并消化,进而在细胞内释放并积累氯膦酸盐。当氯膦酸盐在细胞内的浓度达到一定水平时,便会诱导巨噬细胞发生凋亡。通过这种方式,即利用具有巨噬细胞清除能力的动物模型,我们可以在“体内”环境中深入研究巨噬细胞的功能。
鉴于破骨细胞和巨噬细胞均属于单核吞噬细胞系统(MPS)的范畴,van Rooijen, Nico教授创新性地提出将氯膦酸盐作为“脂质体介导的巨噬细胞自杀技术”中的核心效应分子之一。这一技术利用脂质体作为载体,将效应分子巧妙地引入细胞内并使其积累,从而在20世纪80年代早期被开发出来,用于清除体内器官和组织中的巨噬细胞。尽管后续研究发现了多种其他亲水性分子也适用于此方法作为效应分子,但氯膦酸盐凭借其卓越的功效和极低的毒性,至今仍被视为最佳选择。

微信扫码在线客服