在肿瘤免疫治疗领域,靶向共刺激或共抑制受体已成为突破性策略。DR3(死亡受体3,也称TNFRSF25)作为TNF受体超家族成员,主要在T细胞和NK细胞上表达。其配体TL1A(TNFSF15)则表达于单核细胞、巨噬细胞、树突状细胞及部分非免疫细胞。DR3与TL1A结合后,可调节效应细胞的增殖、活化、凋亡及趋化因子产生,在T细胞介导的免疫应答中发挥关键作用。近年研究表明,抑制DR3-TL1A相互作用在实体瘤治疗中具有显著的治疗潜力。因此,开发能够阻断这一蛋白-蛋白相互作用的抑制剂(小分子或生物制剂)成为药物发现的热点方向。
由艾美捷代理BPS Bioscience推出的DR3:TL1A Inhibitor Screening Assay Kit(货号:82241),正是为高通量筛选和表征DR3-TL1A相互作用抑制剂而设计的完整化学发光检测方案。该试剂盒采用基于ELISA原理的竞争性或直接结合检测模式,以96孔或384孔板形式运行,可快速评估化合物或抗体对DR3与TL1A结合的阻断效果。以下从检测原理、试剂盒组分、操作流程及应用场景等方面进行详细介绍。
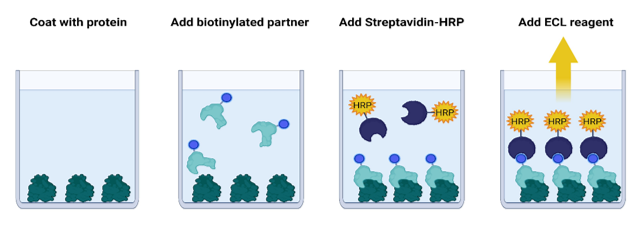
图1:DR3:TL1A抑制剂筛选检测试剂盒工作流程图。
首先,将DR3涂覆在96孔板或384孔板上。接下来,将生物素化的TL1A与DR3一起孵育。最后,用链霉亲和素-辣根过氧化物酶(HRP)处理板,然后加入HRP底物以产生化学发光。化学发光信号与DR3:TL1A的结合成比例
一、检测原理:固相结合-化学发光读出
本试剂盒采用固相蛋白-蛋白相互作用检测模式,核心流程如下:
1. 配体包被:利用试剂盒提供的生物素标记TL1A蛋白(biotin-labeled TL1A,氨基酸72至C端),通过生物素-链霉亲和素相互作用将其固定在预先包被链霉亲和素的微孔板上。这一固定化过程保持了TL1A的天然构象和结合活性。
2. 受体结合:加入纯化的DR3蛋白(氨基酸25-199,即胞外结构域),在优化缓冲液中与固定的TL1A发生特异性结合。若体系中存在抑制剂(小分子或抗体),则会竞争性或变构性地阻断DR3与TL1A的相互作用,导致结合到板上的DR3量减少。
3. 信号检测:洗涤去除未结合的DR3后,加入链霉亲和素标记的辣根过氧化物酶(streptavidin-labeled HRP)。该酶通过链霉亲和素与生物素化TL1A结合(不依赖DR3),因此信号强度理论上应与TL1A的包被量成正比。但为了检测DR3的结合量,实际试剂盒中还需依赖额外的检测抗体。根据BPS Bioscience同类产品设计惯例,该试剂盒包含抗DR3的一抗及HRP标记的二抗,或直接使用HRP标记的抗DR3抗体。用户手册会提供详细步骤。最终加入化学发光底物,HRP催化产生光信号,光强度与结合在板上的DR3量呈正相关。
4. 数据解读:抑制剂存在时,DR3结合减少,光信号降低;无抑制剂时信号最高。通过计算抑制率来评价化合物的阻断效力。
二、试剂盒组分与规格
该试剂盒提供两种规格:96孔板形式(100次反应)和384孔板形式(400次反应),每个试剂盒包含以下核心组分:
生物素标记的TL1A(biotin-labeled TL1A,氨基酸72至C端)
纯化的人源DR3蛋白(氨基酸25-199)
链霉亲和素标记的HRP(streptavidin-labeled HRP)
检测缓冲液(经优化以维持蛋白稳定性和结合特异性)
详细操作说明书
此外,试剂盒中通常包含链霉亲和素预包被的微孔板(未明确写出,但根据“convenient 96-well or 384-well format”及同类产品惯例,板条已包含在内)。所有组分在收货后按指示存储(建议-80°C),自收货之日起6个月内保持最佳性能。
三、应用场景
本试剂盒主要面向两大药物发现需求:
1. 小分子抑制剂或生物制剂的筛选
在药物发现早期,研究者可使用该试剂盒对化合物库或抗体文库进行高通量筛选(HTS),快速识别能够阻断DR3-TL1A相互作用的候选分子。384孔板格式支持自动化工作站,每天可完成数千个样品的初筛。检测体系为均相(结合后洗涤),化学发光信号稳定,Z'因子通常大于0.7,适合高置信度筛选。
2. 抑制剂的滴定与IC50测定
对于初筛获得的阳性化合物,可进一步进行剂量-响应曲线分析。将待测样品稀释为8-12个浓度梯度,按相同流程检测,计算每个浓度的抑制率,使用四参数逻辑回归拟合IC??值。该方法同样适用于抗体药物的亲和力排序及表位竞争分析。
四、实验流程简要说明
以下为典型96孔板操作流程:
1. 试剂准备:将所有组分从-80°C取出,置于冰上解冻。平衡检测缓冲液至室温。准备待测抑制剂稀释系列(建议使用检测缓冲液稀释,保持DMSO终浓度≤1%)。
2. 包被:将生物素标记的TL1A用检测缓冲液稀释至推荐浓度(如0.5-2 ug/mL),每孔加入50 uL,用封板膜覆盖,4°C过夜或室温孵育2小时。或者使用预包被链霉亲和素的板,直接加入生物素-TL1A室温孵育1小时。
3. 洗涤:弃去包被液,每孔加入200 uL PBST,洗涤3次,每次振荡30秒后弃去。
4. 抑制剂与DR3共孵育:每孔加入25 uL检测缓冲液,然后加入25 uL稀释的待测化合物(或对照孔加入缓冲液/已知抑制剂),最后加入25 uL DR3蛋白(终浓度需预实验优化)。室温振荡孵育1-2小时。
5. 检测:洗涤3次后,加入链霉亲和素-HRP(及抗DR3检测抗体,按试剂盒说明稀释),室温孵育30-60分钟。再次洗涤后,加入化学发光底物,立即在酶标仪上读取发光值(积分时间100-500毫秒)。
6. 数据分析:计算抑制率% = (信号_max - 信号_sample) / (信号_max - 信号_min) × 100%,其中信号_max为无抑制剂对照孔,信号_min为无DR3或无TL1A的背景对照孔。使用GraphPad等软件拟合IC??。
五、存储稳定性
该试剂盒所有组分在收货后按指示温度(通常为-80°C)储存,自收货之日起6个月内性能稳定。荧光标记物(如有)需避光保存。建议将生物素-TL1A和DR3蛋白分装为单次使用量,避免反复冻融导致活性下降。
六、文献参考
Xu, W. D., et al., 2022 Front. Immunol. 13: 1-10.
Zwolak, A., et al., 2022 Sci. Rep. 12(1): 20538.

微信扫码在线客服