在DNA损伤修复领域,PARP家族是一类关键的核酶,通过催化多聚ADP-核糖化(PARylation)参与DNA单链断裂修复、基因组稳定性维持及细胞应激响应。PARP2作为该家族的重要成员,虽然仅贡献约10%的总PARP活性,但在DNA修复、氧化应激应答及线粒体片段化中发挥不可替代的作用。基因敲除研究显示,PARP2还参与脂肪生成、精子发生及胸腺细胞存活,并作为雌激素受体(ER)和过氧化物酶体增殖物激活受体(PPAR)的共调节因子。值得注意的是,PARP2在前列腺癌中过表达,并通过FOXA1/AR通路促进疾病进展。临床上已获批的PARP抑制剂(如奥拉帕尼、尼拉帕尼等)同时靶向PARP1和PARP2,但其对PARP2选择性抑制的贡献及潜在的治疗优势仍在深入研究中。因此,开发能够精准、高效检测PARP2酶活性的分析工具,对于靶向PARP2的药物发现及机制研究至关重要。
由艾美捷代理的BPS Bioscience推出的PARP2 Chemiluminescent Assay Kit(货号:80552),正是为满足上述需求而设计的一套完整化学发光检测方案。该试剂盒采用基于组蛋白包被板的ELISA原理,通过检测生物素化ADP-核糖掺入底物的量来定量PARP2的酶活性,适用于小分子抑制剂筛选、酶动力学研究及高通量筛选(HTS)。以下从检测原理、试剂盒组分、操作流程、应用场景及性能特点等方面进行详细介绍。
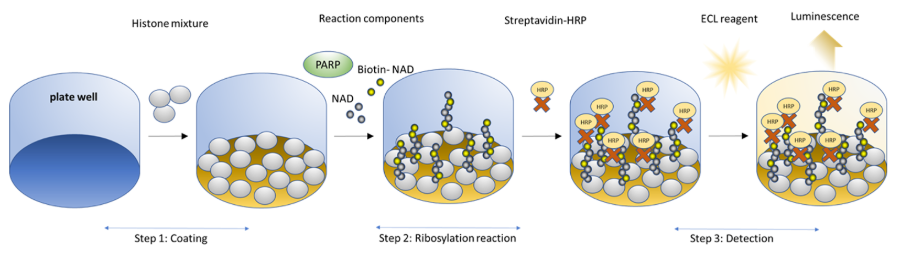
图1. PARP2化学发光检测试剂盒示意图。
组蛋白被涂覆在384孔板上。接下来,在优化的检测缓冲液中,将生物素化的NAD+混合物(称为PARP底物混合物)与PARP2酶和活化的DNA模板一起孵育。然后,用链霉亲和素-HRP处理板,随后加入ELISA ECL底物,产生化学发光,可使用化学发光仪进行测量。化学发光信号与PARP2活性成正比。
一、检测原理:化学发光法定量PARP2的自身PARylation及底物PARylation
本试剂盒采用经典的PARP酶活性ELISA检测模式,核心原理如下:
底物包被:96孔或384孔板预先包被组蛋白或特定核蛋白作为PARP2的底物。组蛋白是PARP家族天然底物,其上的谷氨酸残基可被PARylation修饰。
PARP2反应:加入重组人源PARP2酶(氨基酸2-583,包含催化结构域和DNA结合域)、生物素化NAD?(biotin-NAD?,作为ADP-核糖供体)以及含活化DNA的PARP检测缓冲液。在DNA存在下,PARP2被激活,催化生物素化ADP-核糖单元聚合到组蛋白底物上,同时发生自身PARylation。反应产物为生物素标记的PAR链。
检测:洗涤去除未结合的试剂后,加入链霉亲和素标记的辣根过氧化物酶(Streptavidin-HRP)。链霉亲和素与生物素化PAR链高效结合。再次洗涤后,加入化学发光HRP底物,HRP催化产生光信号。发光强度与固定化PAR链的量呈正比,即与PARP2酶活性呈正比。
抑制剂效应:若体系中加入PARP2抑制剂,酶活性被阻断,生物素化PAR链合成减少,发光信号降低。通过比较抑制剂组与对照组(DMSO或无抑制剂)的发光值,计算抑制率及IC50。
与荧光偏振法或荧光法相比,化学发光检测具有背景极低、信噪比高、动态范围宽的优势,尤其适合需要高灵敏度的筛选应用。同时,该方法为终点法(非实时),可批次处理大量样品,与自动化工作站兼容良好。
二、试剂盒组分与规格
该试剂盒提供两种规格:96孔板形式(100次反应)和384孔板形式(400次反应),每个试剂盒包含以下核心组分:
重组人PARP2酶(氨基酸2-583):纯化自昆虫细胞或大肠杆菌表达系统,经活性验证,确保批次间一致性。
生物素化NAD?(biotin-NAD?):即用型溶液,作为PARylation反应的ADP-核糖来源。
PARP检测缓冲液:含有活化DNA(如剪切的鲑鱼精DNA)及必要的辅因子(Mg??、DTT等),以激活PARP2并维持其催化活性。
链霉亲和素-HRP:浓缩液,使用前需按说明书稀释。
化学发光底物:HRP的发光底物(如鲁米诺/过氧化物溶液)。
10×洗涤缓冲液:需稀释后使用。
封闭缓冲液:用于减少非特异性结合。
详细操作说明书:包含包被步骤、反应条件及数据分析模板。
所有组分在收货后按指示存储(通常为-80°C或-20°C,具体以说明书为准),自收货之日起6个月内保持最佳性能。生物素化NAD?和链霉亲和素-HRP需避免反复冻融。
三、实验流程简要说明
以下为典型96孔板操作流程(试剂盒通常已提供预包被组蛋白的板,或需用户自行包被,以说明书为准):
1. 试剂准备
从-80°C取出PARP2酶、生物素化NAD?、检测缓冲液等,置于冰上解冻。
准备待测抑制剂:用检测缓冲液或DMSO稀释至所需浓度(建议设置10个浓度梯度,2倍或3倍倍比稀释)。注意最终DMSO浓度不得超过1%(见禁忌说明)。
稀释洗涤缓冲液至1×工作浓度。
2. 反应体系构建
使用提供的预包被组蛋白微孔板(若未预包被,需先用组蛋白包被过夜,然后封闭)。
每孔加入50 uL检测缓冲液(含活化DNA)。
加入10 uL稀释的PARP2酶(推荐起始浓度0.5–5 nM,需预实验优化,使信号处于线性区间)。
加入10 uL待测抑制剂或对照(缓冲液/DMSO/阳性对照如奥拉帕尼、他拉唑帕尼等)。
室温预孵育10分钟。
加入10 uL生物素化NAD?(终浓度通常为0.5–2 uM)。
用封板膜覆盖,室温或30°C孵育30–60分钟(使PARylation反应充分进行)。
3. 检测步骤
弃去反应液,每孔加入200 uL 1×洗涤缓冲液,洗涤3次。
加入100 uL稀释的链霉亲和素-HRP(按说明书比例稀释),室温孵育30分钟。
再次洗涤3次。
加入100 uL化学发光底物,立即使用发光酶标仪读取发光值(RLU),积分时间0.5–1秒。
4. 数据分析
四、应用场景
本试剂盒主要面向以下两大类核心应用:
1. PARP2小分子抑制剂的筛选与IC50测定
2. 酶动力学研究与作用机制解析
五、存储稳定性与运输条件
试剂盒采用-80°C干冰运输。收货后,PARP2酶和生物素化NAD?应立即存放于-80°C;链霉亲和素-HRP和化学发光底物通常存放于-20°C(避光);检测缓冲液和洗涤缓冲液可于4°C保存。建议将PARP2酶分装为单次使用量(如2 uL/管),避免反复冻融。在正确存储条件下,所有组分自收货之日起6个月内性能稳定。
文献参考:
Gui B., et al., 2019 Proc Natl Acad Sci USA 116 (29): 14573-14582.

微信扫码在线客服