氧化应激与炎症反应是多种慢性疾病(包括神经退行性疾病、心血管疾病、糖尿病及癌症)的核心病理机制之一。在细胞对抗氧化应激的过程中,转录因子Nrf2(核因子红细胞2相关因子2)发挥着关键的“主调节器”作用。正常情况下,Nrf2在细胞质中被Keap1(Kelch样ECH关联蛋白1)结合并锚定,Keap1作为E3泛素连接酶复合物的底物识别亚基,持续介导Nrf2的泛素化降解,使其维持在较低水平。当细胞暴露于氧化应激或亲电试剂时,Keap1的关键半胱氨酸残基被修饰,构象发生变化,导致Nrf2从Keap1上释放并转位进入细胞核。入核后的Nrf2与ARE(抗氧化反应元件)结合,启动一系列抗氧化蛋白和II相解毒酶(如HO-1、NQO1、GCLC等)的表达,从而保护细胞免受氧化损伤。
鉴于Nrf2/Keap1信号轴在细胞保护中的核心地位,该通路已成为药物发现的明星靶点。激活Nrf2(通过破坏Keap1-Nrf2相互作用)可用于治疗以氧化应激为特征的疾病,如慢性肾病、慢性阻塞性肺病、多发性硬化症等;而在某些癌细胞中,Nrf2的持续激活则促进肿瘤存活和化疗耐药,此时恢复Keap1功能或抑制Nrf2则成为治疗策略。因此,筛选能够阻断Keap1与Nrf2结合的小分子抑制剂,对于开发新型抗氧化药物或辅助化疗增敏剂均具有重要意义。
由艾美捷代理BPS Bioscience推出的Keap1:Nrf2 Inhibitor Screening Assay Kit(货号:72020),正是为满足上述需求而设计的一套完整荧光偏振(Fluorescence Polarization, FP)检测方案。该试剂盒采用96孔板格式,通过监测荧光标记Nrf2肽段与Keap1蛋白结合后旋转运动性的变化,快速、定量地评估化合物对Keap1:Nrf2相互作用的阻断能力,适用于高通量筛选及IC??测定。以下从检测原理、试剂盒组分、操作流程、应用场景及性能特点等方面进行详细介绍。
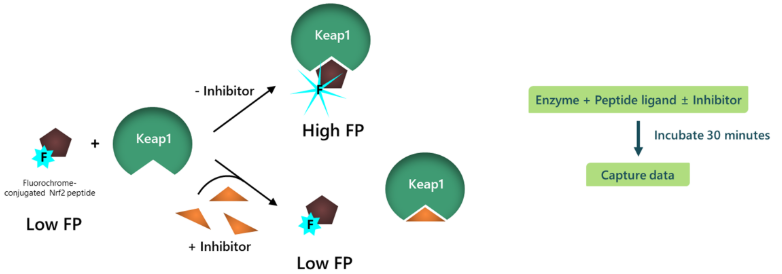
图1. Keap1:Nrf2抑制剂筛选检测试剂盒示意图。
一、检测原理:荧光偏振法监测蛋白-肽段相互作用
荧光偏振是一种基于分子旋转运动性变化来研究分子间相互作用的经典技术,具有均相、无需分离、实时检测等突出优势。其核心原理如下:
当一个小分子荧光团(如荧光素)被偏振光激发时,发射光的偏振程度与其在激发态寿命内的旋转速度密切相关。小分子物质(如自由的荧光标记肽段)旋转速度快,发射光偏振度低;而大分子复合物(如荧光肽段与较大的Keap1蛋白结合后)旋转速度显著减慢,发射光偏振度升高。偏振值通常以毫偏单位(mP)表示。
在本试剂盒中:
荧光标记的Nrf2肽段:该肽段包含Nrf2与Keap1结合所必需的核心基序——ETGE基序,其C端或N端共价连接荧光基团(如FAM)。该肽段分子量较小(约2–3 kDa),自由状态时偏振值较低。
Keap1蛋白:重组人源Keap1蛋白(包含其Kelch结构域,该结构域负责识别Nrf2的ETGE基序)。Keap1分子量约为70 kDa(全长)或Kelch结构域约35 kDa,远大于荧光肽段。
结合反应:当荧光Nrf2肽段与Keap1蛋白结合后,形成分子量约为肽段+Keap1的复合物,旋转速度下降,荧光偏振值显著升高(通常从约50 mP上升至150–200 mP)。
抑制剂效应:若待测化合物能够阻断Keap1与Nrf2肽段的相互作用,则荧光肽段无法被Keap1捕获,保持自由状态,偏振值维持在较低水平。通过比较加抑制剂前后偏振值的变化,即可计算抑制率。
这一检测模式直接评估化合物对蛋白-蛋白相互作用的破坏能力,而非间接测量下游功能变化,因此具有高特异性、高灵敏度及良好的可重复性,非常适合作为先导化合物筛选的主要方法。
二、试剂盒组分与规格
该试剂盒为96孔板格式,包含足够进行100次结合反应的全部核心组分:
纯化的Keap1蛋白:重组人源Keap1,通常为全长或包含Kelch结构域的活性片段,经质控验证具有Nrf2肽段结合活性。
荧光标记的Nrf2肽段:包含ETGE基序,荧光基团为FAM(激发/发射约485/535 nm),避光保存。
检测缓冲液:经优化的缓冲体系(含适当盐浓度、pH稳定剂及去垢剂),以维持蛋白稳定性并降低非特异性结合。
详细操作说明书:包含蛋白和肽段的推荐工作浓度、稀释方法及数据分析模板。
所有组分在收货后按指示存储(通常为-80°C),自收货之日起6个月内保持最佳性能。荧光肽段对光敏感,需避光保存并避免反复冻融。
三、实验流程简要说明
以下为典型96孔板单次反应的操作步骤(半面积板或常规板均可):
1. 试剂准备
从-80°C取出Keap1蛋白、荧光Nrf2肽段和检测缓冲液,置于冰上解冻。
平衡检测缓冲液至室温。荧光肽段解冻后短暂离心,置于冰上避光保存。
准备待测抑制剂:用DMSO或检测缓冲液稀释至所需浓度(建议设置10个浓度梯度,3倍或2倍倍比稀释)。
2. 反应体系构建(每孔总体积50–100 μL,以说明书为准)
加入检测缓冲液补足体积。
加入荧光Nrf2肽段至终浓度(通常为5–20 nM)。
加入待测抑制剂或对照(空白对照为缓冲液,阴性对照为DMSO,阳性对照可使用已知Keap1-Nrf2抑制剂如ML385或KI696等,但需用户自备)。
加入Keap1蛋白至终浓度(通常为50–200 nM,需预实验确定EC??浓度)。
推荐先混合肽段和抑制剂,最后加入Keap1启动反应。
3. 孵育与读数
用封板膜覆盖96孔板,室温避光孵育30–60分钟,使反应达到平衡。
使用具备荧光偏振检测模块的酶标仪,设定激发波长485 nm,发射波长535 nm。分别读取平行偏振(S)和垂直偏振(P)信号。
计算每孔的偏振值(mP):
四、存储稳定性与运输条件
试剂盒采用-80°C干冰运输。收货后,Keap1蛋白和荧光肽段应立即存放于-80°C,检测缓冲液可于-20°C或4°C短期保存。荧光肽段需严格避光。建议将蛋白和肽段分装为单次使用量,避免反复冻融。在正确存储条件下,所有组分自收货之日起6个月内性能稳定。
五、文献参考
Inoyama, D., et al. 2012. J. Biomol. Screening 17(4): 435-447

微信扫码在线客服