FBXL10(F-box and leucine-rich repeat protein 10),又称KDM2B、JHDM1B或CXXC2,是一种组蛋白赖氨酸去甲基化酶,能够特异性催化组蛋白H3第4位三甲基赖氨酸(H3K4me3)和第36位二甲基赖氨酸(H3K36me2)的去甲基化反应。作为多梳抑制复合物(PRC)的组成部分,FBXL10在细胞增殖、分化和迁移中发挥关键调控作用。研究表明,FBXL10在弥漫性大B细胞淋巴瘤(DLBCL)中具有致癌活性,但在某些细胞类型中又表现为肿瘤抑制功能,提示其作用具有细胞类型依赖性。深入解析FBXL10的生物学功能及其在癌症发生发展中的双重角色,将为肿瘤治疗提供新靶点和新策略。
为满足科研人员在FBXL10酶活性检测、抑制剂筛选及药物发现中的需求,由艾美捷代理BPS Bioscience公司推出的FBXL10 (KDM2B) 均相检测试剂盒(货号:50610)提供了一套基于AlphaLISA技术的高灵敏度、高通量兼容的解决方案。该试剂盒以96孔或384孔板格式提供,包含纯化的重组FBXL10酶、特异性抗体、生物素化底物及优化缓冲液,支持100次或400次酶反应,适用于酶动力学研究及小分子抑制剂的高通量筛选(HTS)。
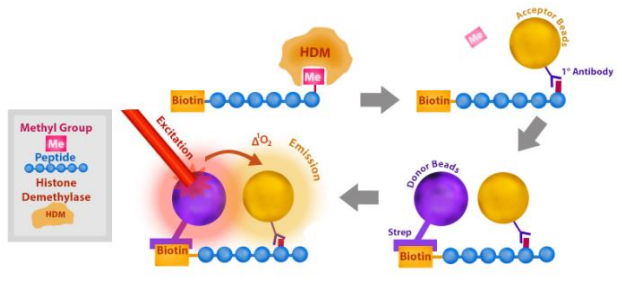
图1:FBXL10(KDM2B)均相检测试剂盒原理。
首先,将含有FBXL10酶的样本与生物素化底物一起孵育。接着,加入受体珠和一抗,然后加入供体珠。α计数与去甲基酶活性成正比。
一、检测原理:基于AlphaLISA的均相免洗技术
本试剂盒采用AlphaLISA(Amplified Luminescent Proximity Homogeneous Assay) 技术,这是一种基于化学发光的均相检测方法,无需洗涤步骤,具有极高的灵敏度和宽广的动态范围。
检测流程分为两个关键步骤:
第一步:酶催化去甲基化反应。 将重组FBXL10酶与生物素化组蛋白H3肽底物(含H3K4me3或H3K36me2修饰)共同孵育。在酶活性存在下,底物上的甲基被移除,产生去甲基化的肽产物。
第二步:AlphaLISA信号检测。 反应结束后,依次加入:
兔源一抗:特异性识别去甲基化后的表位(即仅在甲基被移除后暴露的抗原表位)。
AlphaLISA Anti-Rabbit IgG Acceptor Beads(受体微球):偶联有抗兔IgG抗体。
AlphaScreen Streptavidin Donor Beads(供体微球):通过链霉亲和素与生物素化底物结合。
当底物被FBXL10去甲基化后,一抗与去甲基化表位结合,进而通过二抗将受体微球招募至同一复合物。此时,供体微球(结合于底物的生物素端)与受体微球(结合于抗体端)在空间上相互靠近。在680 nm激光激发下,供体微球产生单线态氧;若两种微球距离小于200 nm,单线态氧可传递至受体微球,触发其发出615 nm的化学发光信号。发光强度与FBXL10的去甲基化酶活性成正比。若化合物抑制FBXL10活性,去甲基化产物减少,一抗无法结合,受体微球不能被招募,信号降低。
关键优势:AlphaLISA技术无需洗涤,操作简单(“加样-混合-孵育-读数”),背景极低,灵敏度可达fmol级,动态范围超过4个数量级,完美兼容自动化高通量筛选。
二、试剂盒核心组分与设计优势
1. 即用型完整组分(需自购Alpha微球)
试剂盒提供以下核心组分(注意:AlphaLISA受体微球和AlphaScreen供体微球需单独向PerkinElmer购买):
纯化的重组人FBXL10(KDM2B)酶:保留完整去甲基化酶活性。
生物素化组蛋白H3肽底物:含特定甲基化修饰(H3K4me3或H3K36me2)。
兔源一抗:特异性识别去甲基化表位。
10× 检测缓冲液:优化pH和离子组成,确保酶反应及AlphaLISA信号稳定。
微孔板:可选OptiPlate-96或OptiPlate-384(PerkinElmer)。
2. 96孔/384孔双规格,灵活适配不同通量
该试剂盒提供96孔(100次酶反应)和384孔(400次酶反应)两种规格,用户可根据实验规模灵活选择:
96孔规格:适合常规实验、方法开发及中小规模抑制剂筛选。
384孔规格:适合高通量筛选(HTS),单位反应成本更低,与自动化移液工作站完美兼容。
3. 内置对照(建议自行配置)
虽然试剂盒本身未提供阳性对照抑制剂,但研究人员可使用已知的组蛋白去甲基化酶抑制剂(如CPI-455,针对KDM5家族,但对FBXL10有参考价值)或自行验证的化合物作为阳性对照。建议在每次实验中设置无酶对照(背景信号)和无抑制剂对照(最大信号),以确保数据的可靠性。
三、应用场景与科研价值
1. FBXL10抑制剂的高通量筛选
FBXL10在DLBCL、胶质瘤等多种肿瘤中高表达,其去甲基化酶活性促进肿瘤细胞增殖和迁移。利用该试剂盒,研究人员可以:
在96孔或384孔板中快速筛选数千个化合物,评估其对FBXL10去甲基化酶活性的抑制效果。
通过剂量-反应曲线测定IC50值,比较不同化合物的抑制效力。
筛选FBXL10选择性抑制剂(与其他KDM家族成员进行正交筛选),为开发靶向FBXL10的抗肿瘤药物提供先导化合物。
2. 酶动力学研究
利用试剂盒中的纯化重组酶和生物素化底物,研究人员可以:
通过改变底物浓度,测定FBXL10的米氏常数(Km)及最大反应速率(Vmax)。
分析不同突变体(如与癌症相关的FBXL10突变)对酶活性的影响。
研究FBXL10与其他PRC复合物组分(如RING1B、BMI1)相互作用对酶活性的调节。
3. 构效关系(SAR)研究
在药物化学优化阶段,该试剂盒可用于评估系列化合物(如小分子类似物、PROTAC分子)对FBXL10的抑制活性,快速筛选出活性最优的候选化合物,指导药物设计。
4. 表观遗传调控机制研究
FBXL10不仅催化组蛋白去甲基化,还通过其CXXC结构域结合非甲基化CpG岛,参与基因转录调控。利用该试剂盒,研究人员可以定量分析不同细胞状态(如分化、应激、药物处理)下FBXL10的酶活性变化,揭示其在表观遗传调控网络中的功能。
四、操作要点(典型步骤)
1. 准备试剂:将FBXL10酶、生物素化底物、一抗及检测缓冲液从-80°C取出,冰上融化。注意避光保存Alpha微球。
2. 配制反应混合液:根据说明书稀释FBXL10酶至工作浓度。
3. 酶反应:在微孔板中加入检测缓冲液、待测化合物(或抑制剂)、FBXL10酶和生物素化底物,混匀后37°C孵育60-120分钟。
4. 一抗结合:加入兔源一抗,室温孵育30-60分钟。
5. Alpha微球加入:在避光条件下加入AlphaLISA受体微球和AlphaScreen供体微球(需预先稀释至工作浓度),室温避光孵育30-60分钟。
6. 读数:使用AlphaScreen兼容的荧光微孔板读数仪,在680 nm激发波长下检测615 nm发射光强度。
7. 数据分析:计算抑制率 =(1 - 样品信号值 / 无抑制剂对照信号值)× 100%,使用非线性回归拟合IC50曲线。
五、文献参考
Iwase S., et al., 2007 Cell 128(6):1077-1088.
Zhao X., et al., 2018 Cell Death Dis. 9(2):46.

微信扫码在线客服