细胞黏附分子(CAMs)
CAMs是参与细胞与其他细胞或细胞外基质(ECM)结合的跨膜受体蛋白。根据其结构,CAMs可分为四大类:整合素、钙黏蛋白、选择素和免疫球蛋白超家族细胞黏附分子(IgCAMs)(Ruan et al., 2022)。
整合素是由α和β亚基组成的异二聚体蛋白,介导细胞与ECM之间的相互作用(例如,CD11b/ITGAM、CD11c/ITGAX)。 钙黏蛋白是钙依赖性的单次跨膜蛋白,其特征是胞外结构域具有多个钙黏蛋白重复序列。经典钙黏蛋白具有五个胞外钙黏蛋白(EC)重复序列,并根据其结合位点的结构分为I型或II型。I型钙黏蛋白的例子包括E-钙黏蛋白/钙黏蛋白1、N-钙黏蛋白/钙黏蛋白2和P-钙黏蛋白/钙黏蛋白3,而II型钙黏蛋白的例子包括VE-钙黏蛋白/钙黏蛋白5和K-钙黏蛋白/钙黏蛋白6。非经典钙黏蛋白具有不同数量的EC重复序列(Sotomayor et al., 2015)。 选择素是钙依赖性的单链跨膜糖蛋白,通过凝集素-糖相互作用与碳水化合物结合(例如,P-选择素、E-选择素)。
IgCAMs的定义是具有与Ig序列相似的区域,称为Ig结构域(例如,细胞间黏附分子1(ICAM1)、神经细胞黏附分子1(NCAM1)、血管细胞黏附分子1(VCAM1)、血小板内皮细胞黏附分子1(CD31/PECAM1))。 血管内皮细胞上的CAMs 血管内皮细胞表达对于血管功能、免疫监视和炎症至关重要的CAMs。一些CAMs,如CD31/PECAM1、ICAM1和ICAM2,是组成性表达的,而其他CAMs,如VCAM1和P-选择素,在基础状态下表达水平极低或不表达。当受到促炎细胞因子(例如,TNFα、IL-1β)或细菌成分(例如,LPS)刺激时,CAMs会在内皮细胞上被诱导表达。其调控程度从中等(如CD31和ICAM2)到非常强(如VCAM1和ICAM1)不等。值得注意的是,ICAM1和VCAM1的上调是内皮功能障碍的标志,并正在被探索作为心血管风险评估的潜在生物标志物(Kaur et al., 2022)。 ICAM1主要表达于内皮细胞、免疫细胞和上皮细胞(Bui et al., 2021)。VCAM1主要存在于内皮细胞上(Osborn et al., 1989)。在高炎症和慢性疾病条件下,VCAM1也可以在其他细胞表面表达,包括组织巨噬细胞、树突状细胞、骨髓成纤维细胞、成肌细胞、卵母细胞、库普弗细胞、支持细胞和癌细胞。ICAM1和VCAM1是参与白细胞跨越血管内皮的黏附和跨迁移的重要分子(Kong et al., 2018)。
ICAM1和VCAM1在白细胞外渗中的作用
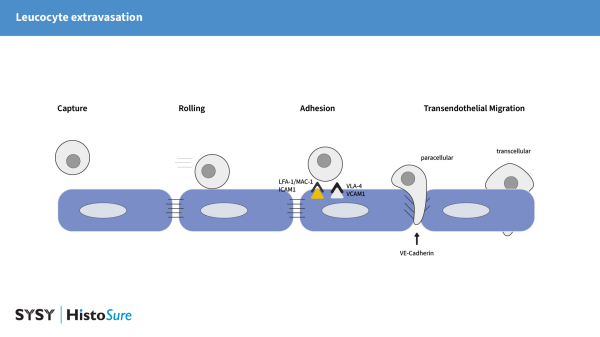
图1:白细胞穿越内皮屏障的示意图。
跨内皮迁移受到多种黏附分子的严格调控。在捕获、滚动和牢固黏附之后,白细胞可以经旁细胞途径或跨细胞途径穿越内皮屏障。
白细胞外渗是炎症反应中的关键过程,因为先天性和适应性免疫系统的有效激活都需要白细胞从血液中退出并进入受影响的组织。这一多步骤过程包括连续的时相:初始捕获、沿内皮滚动、牢固黏附,以及最终的跨内皮迁移(TEM),后者可通过旁细胞或跨细胞途径发生(Sullivan and Muller, 2014, Salminen et al., 2020)。
捕获与滚动:内皮细胞上的P-选择素和E-选择素与白细胞结合,介导初始的栓系和沿血管壁的滚动。 牢固黏附:ICAM1和VCAM1与白细胞上的整合素结合。ICAM1通过与淋巴细胞功能相关抗原1(LFA-1,由CD11a和CD18组成的异二聚体)和巨噬细胞-1抗原(Mac-1,由CD11b和CD18组成的异二聚体)的相互作用,参与白细胞与内皮细胞顶面的牢固黏附。VCAM1通过与非常晚期抗原-4(VLA-4,由CD49d和CD26组成的异二聚体)的结合,参与单核细胞的牢固黏附。 旁细胞TEM:ICAM1的刺激导致VE-钙黏蛋白的磷酸化,连接松动和内皮通透性增加。 跨细胞TEM:PECAM1和CD99参与白细胞与内皮细胞之间的同型相互作用。这些相互作用触发膜从LBRC(侧缘回收区室)动员,包裹迁移的白细胞,促进跨迁移。 VCAM1和ICAM1在疾病中的作用 炎症细胞因子,包括TNFα、IL-1β和IFNγ,不仅在内皮细胞上,而且在其他细胞类型(例如,成纤维细胞和炎症性巨噬细胞)上强烈上调ICAM1和VCAM1的表达(Hosokawa et al., 2006, Wiesolek et al., 2020)。例如,在感染弓形虫(T.)gondii的小鼠肝脏中,肝窦内皮细胞和多灶性单核细胞聚集处可见ICAM1和VCAM1表达水平升高(图2)。
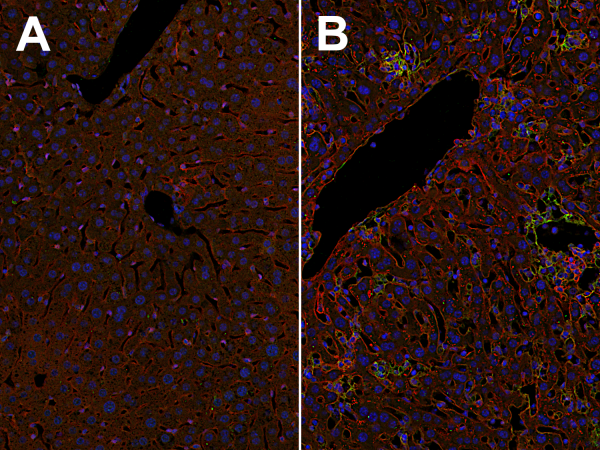
图2:感染T. gondii的小鼠肝脏中肝窦内皮细胞和多灶性单核细胞聚集处ICAM1和VCAM1水平升高。对未感染小鼠(A)和T. gondii感染小鼠(B)的福尔马林固定石蜡包埋(FFPE)小鼠肝脏切片进行间接免疫染色,使用兔抗ICAM1抗体(货号HS-532 003,稀释度1:500,红色)和豚鼠抗VCAM1抗体(货号HS-470 004,稀释度1:500,绿色)。细胞核通过DAPI染色显示(蓝色)。
不出所料,这两种分子均与多种炎症性和退行性疾病的进展有关。ICAM1调控广泛的细胞功能,包括T细胞活化、巨噬细胞极化、活性氧(ROS)产生和定向细胞迁移。ICAM1信号失调与癌症、脓毒症、多发性硬化症和心血管疾病相关(Haydinger et al., 2023, Kaur et al., 2022)。ICAM1还可作为恶性疟原虫和弓形虫某些蛋白的受体(Haydinger et al., 2023)。其在肿瘤细胞上的表达使ICAM1成为癌症治疗的一个引人注目的靶点(Guo et al., 2014, Min et al., 2017)。VCAM1也与多种病理状况相关,如类风湿性关节炎、哮喘、移植排斥反应和不同类型的癌症(Kong et al., 2018)。因此,VCAM1是自身免疫性和癌性病理的一个有前景的治疗靶点(Pickett et al., 2023, Pickett et al., 2025)。
中枢神经系统受累 在中枢神经系统(CNS)中,ICAM1和VCAM1是神经炎症的关键介质,在调节血脑屏障(BBB)通透性方面发挥核心作用。ICAM1在血脑屏障内的反应性星形胶质细胞和内皮细胞上显著表达,参与多种神经退行性疾病的发生和发展。同样,VCAM1在炎症条件下于脑血管内皮上被上调。值得注意的是,在感染SARS-CoV2和弓形虫的小鼠脑血管中均观察到ICAM1和VCAM1的表达升高(Yang et al., 2022, Silva et al., 2010)(图3和图4)。

图3:对未感染小鼠(A)和SARS-CoV2感染小鼠(B)的福尔马林固定石蜡包埋(FFPE)小鼠脑切片进行间接免疫染色,使用兔抗ICAM1抗体(货号HS-532 003,稀释度1:1000,DAB,棕色)。细胞核通过苏木精染色显示(蓝色)。
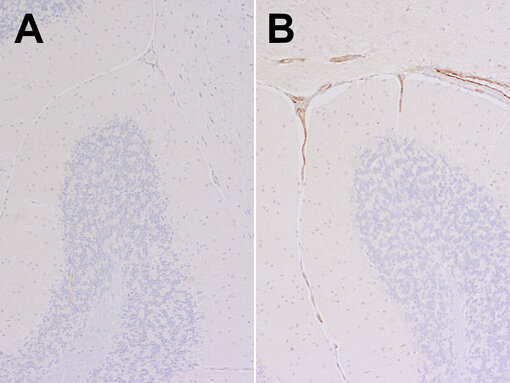
图4:对未感染小鼠(A)和SARS-CoV2感染小鼠(B)的福尔马林固定石蜡包埋(FFPE)小鼠脑(小脑)切片进行间接免疫染色,使用豚鼠抗VCAM1抗体(货号HS-470 004,稀释度1:750,DAB,棕色)。细胞核通过苏木精染色显示(蓝色)。
新兴研究已确定ICAM1与铁死亡之间存在关联——铁死亡是一种由铁依赖性脂质过氧化驱动的受调控细胞死亡形式,越来越多地被认为是帕金森病(PD)发病机制中的 contributing factor。ICAM1表达升高在晚年抑郁症病例中也有报道,突显了其在神经精神障碍中的更广泛作用(Miller et al., 2024)。同样,在PD患者的血清和血浆中检测到VCAM1水平升高(Zheng et al., 2022)。此外,早期脑转移(BM)邻近内皮细胞中VCAM1的表达提示其可能参与BM进展,并将其作为靶向治疗策略的候选分子(Corroyer-Dulmon et al., 2020)。
可溶性形式及其临床意义 ICAM1和VCAM1不仅以其膜结合形式存在,还以可溶性异构体——sICAM1和sVCAM1——的形式存在,后者通过蛋白水解切割产生。值得注意的是,sVCAM1已被证明可直接损害血脑屏障(BBB)的完整性(Haarmann et al., 2015)。这些黏附分子的可溶性形式目前正在被探索作为全身性炎症、血管损伤和BBB破坏的有前景的生物标志物(Videm and Albrigtsen, 2008, Varona et al., 2019, Uzawa et al., 2011)。此外,sICAM1和sVCAM1水平升高与多种神经精神障碍相关(Meixensberger et al., 2021)。
结论 ICAM1和VCAM1在调控炎症反应中发挥核心作用,是心血管疾病、帕金森病和抑郁症等疾病的潜在治疗靶点和生物标志物。
Cat. No. | Product Description | Application | Quantity |
HS-532 003 | ICAM1, rabbit, polyclonal, affinity purified | WB IHC IHC-P | 50 ?g |
HS-470 003 | VCAM1, rabbit, polyclonal, affinity purified | IHC IHC-P | 50 ?g |
HS-470 004 | VCAM1, Guinea pig, polyclonal, antiserum | WB IHC IHC-P | 100 ?l |
文献参考:
Bui et al., 2021. ICAM-1: A master regulator of cellular responses in inflammation, injury resolution, and tumorigenesis. PMID: 32182390
Corroyer-Dulmon et al., 2020. VCAM-1 targeted alpha-particle therapy for early brain metastases. PMID: 31538194
Guo et al., 2014. ICAM-1 as a molecular target for triple negative breast cancer. PMID: 25267626
Haarmann et al., 2015. Soluble VCAM 1 impairs human brain endothelial barrier integrity via integrin α 4 transduced outside in signalling. PMID: 25814153
Haydinger et al., 2023. Intercellular Adhesion Molecule 1: More than a Leukocyte Adhesion Molecule. PMID: 37237555
Hosokawa et al., 2006. Cytokines differentially regulate ICAM-1 and VCAM-1 expression on human gingival fibroblasts. PMID: 16734619
Kaur et al., 2022. Novel insights on the role of VCAM-1 and ICAM-1: Potential biomarkers for cardiovascular diseases. PMID: 36408439
Kong et al., 2018. Emerging Roles of Vascular Cell Adhesion Molecule-1 (VCAM-1) in Immunological Disorders and Cancer. PMID: 29614819
McCray Jr et al., 2007. Lethal infection in K18-hACE2 mice infected with SARS-CoV. PMID: 17079315
Meixensberger et al., 2021. Upregulation of sICAM-1 and sVCAM-1 Levels in the Cerebrospinal Fluid of Patients with Schizophrenia Spectrum Disorders. PMID: 34206599
Miller et al., 2024. Intercellular Adhesion Molecule 1 (ICAM-1): An Inflammatory Regulator with Potential Implications in Ferroptosis and Parkinson’s Disease. PMID: 39329738
Min et al., 2017. CAR T Therapy Targeting ICAM-1 Eliminates Advanced Human Thyroid Tumors. PMID: 29025766
Osborn et al., 1989. Direct expression cloning of vascular cell adhesion molecule 1, a cytokine-induced endothelial protein that binds to lymphocytes. PMID: 2688898
Pickett et al., 2023. Targeting endothelial vascular cell adhesion molecule-1 in atherosclerosis: drug discovery and development of vascular cell adhesion molecule-1-directed novel therapeutics. PMID: 37595265
Pickett et al., 2025. VCAM-1 as a common biomarker in inflammatory bowel disease and colorectal cancer: unveiling the dual anti-inflammatory and anti-cancer capacities of anti-VCAM-1 therapies. PMID: 40095109
Ruan et al., 2022. Mechanisms of Cell Adhesion Molecules in Endocrine-Related Cancers: A Concise Outlook. PMID: 35464064
Salminen et al., 2020. In vitro Studies of Transendothelial Migration for Biological and Drug Discovery. PMID: 35047883
Silva et al., 2010. Toxoplasma gondii: The severity of toxoplasmic encephalitis in C57BL/6 mice is associated with increased ALCAM and VCAM-1 expression in the central nervous system and higher blood–brain barrier permeability. PMID: 20434443
Sotomayor et al., 2015. Sorting Out a Promiscuous Superfamily: Towards Cadherin Connectomics. PMID: 24794279
Sullivan and Muller, 2014. Neutrophil and Monocyte Leukocyte recruitment by PECAM, CD99 and other molecules via the LBRC. PMID: 24337626
Uzawa et al., 2011. Markedly Elevated Soluble Intercellular Adhesion Molecule 1, Soluble Vascular Cell Adhesion Molecule 1 Levels, and Blood-Brain Barrier Breakdown in Neuromyelitis Optica. PMID: 21747031
Varona et al., 2019. Soluble ICAM 1 and VCAM 1 Blood Levels Alert on Subclinical Atherosclerosis in Non Smokers with Asymptomatic Metabolic Syndrome. PMID: 31349950
Videm and Albrigtsen, 2008. Soluble ICAM-1 and VCAM-1 as Markers of Endothelial Activation. PMID: 18363595
Wiesolek et al., 2020. Intercellular Adhesion Molecule 1 Functions as an Efferocytosis Receptor in Inflammatory Macrophages. PMID: 32035057
Yang et al., 2022. SARS-CoV-2 productively infects human brain microvascular endothelial cells. PMID: 35705998
Zheng et al., 2022. Increased PRR14 and VCAM-1 level in serum of patients with Parkinson's disease. PMID: 36247752

微信扫码在线客服