什么是TL1A:DR3通路?
TL1A(又称VEGI-251或TNFSF15)是肿瘤坏死因子(TNF)超家族成员,与其受体死亡受体3(DR3)共同构成一条关键的免疫调控通路。TL1A以三聚体II型跨膜蛋白形式表达,经金属蛋白酶(如TACE)切割后释放为可溶性蛋白,与DR3结合启动下游信号级联。该通路是先天免疫与适应性免疫交叉对话的核心介导者,调控免疫细胞的活化、分化及细胞因子产生,在免疫耐受、组织修复和宿主防御中发挥多效性作用。
信号机制:双向调控,一念成佛一念成魔
促炎/存活通路:TL1A结合DR3后,通过TRADD招募TRAF2和RIP1等接头蛋白,激活NF-κB和AP-1转录因子,驱动T细胞增殖、促炎细胞因子产生及辅助性T细胞亚群分化。
凋亡/坏死通路:DR3也可通过FADD募集RIP1/RIP3,激活caspase通路,诱导细胞凋亡或程序性坏死。
天然刹车系统:诱骗受体DcR3作为可溶性竞争抑制剂,与TL1A结合阻断其与DR3的相互作用,有效抑制TL1A介导的信号传导,维持免疫稳态。
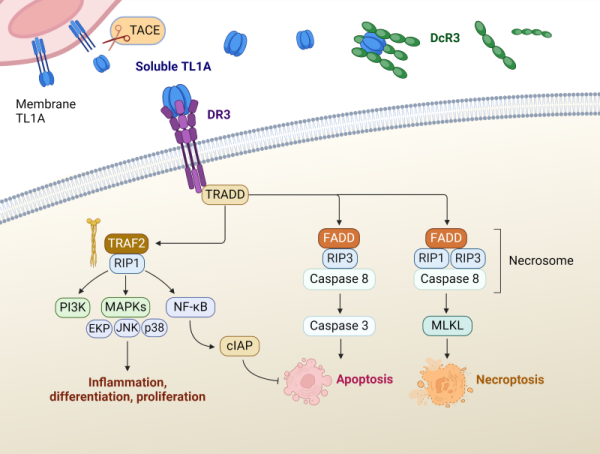
图1. TL1A 与 DR3 的信号通路
研究意义:从自身免疫到肿瘤的广阔疆域
在健康状态下,TL1A:DR3通路参与免疫监视和感染清除;但在病理状态下,其失调与多种疾病密切相关:
自身免疫病:类风湿关节炎、炎症性肠病(IBD)、银屑病等
肿瘤微环境:T细胞耗竭导致抗肿瘤免疫应答受损
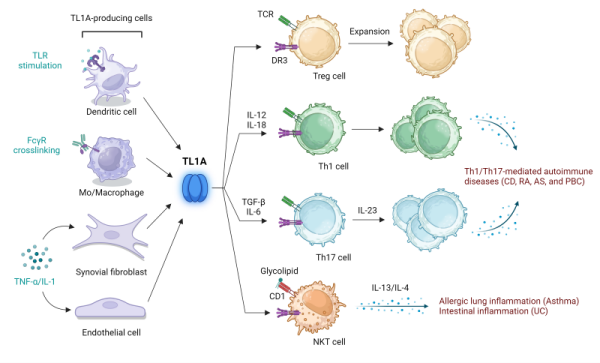
图2. TL1A 能够将先天免疫反应与适应性免疫反应连接起来,并且是自身免疫和炎症性疾病的关键驱动因素,这些疾病包括克罗恩病(CD)、类风湿性关节炎(RA)、强直性脊柱炎(AS)、原发性胆汁性肝硬化(PBC)、哮喘以及溃疡性结肠炎(UC)。
治疗策略:双向调控的精准医学
阻断策略(自身免疫/炎症)
使用抗TL1A或抗DR3抗体阻断信号传导,可恢复免疫平衡、减轻疾病严重程度。相比传统免疫抑制剂,具有更高特异性和更低副作用风险。目前已在临床前研究和早期临床试验中显示出令人鼓舞的结果。
激活策略(肿瘤免疫)
在T细胞功能低下的肿瘤微环境中,DR3激动剂可协同刺激耗竭T细胞,恢复其抗肿瘤活性。与PD-1/PD-L1免疫检查点抑制剂联合使用,有望克服单药治疗耐药的难题,实现"1+1>2"的增效作用。
BPS Bioscience关键研究工具
货号 | 名称 | 应用 |
DR3:TL1A抑制剂筛选试剂盒 | 筛选并鉴定DR3与TL1A相互作用的抑制剂 | |
82160 | DcR3:TL1A抑制剂筛选试剂盒 | 筛选并鉴定DcR3与TL1A相互作用的抑制剂 |
78811 | TL1A 反应型荧光素酶报告基因 Jurkat 细胞系 | 测定可溶性 TL1A 活性;在细胞检测格式中筛选抗TL1A 抗体 |
101729 | TL1A中和抗体 | 适用于在ELISA及细胞实验中研究 TL1A 的中和作用 |
101880 | TL1A重组蛋白(His标签,Avi标签) | 由于存在糖基化修饰,该蛋白质在SDS-PAGE 测定中呈现出更高的分子量 |
抑制剂筛选试剂盒可用于筛选和验证与 DR3:TL1A 和 DcR3:TL1A 交互作用的抑制剂。这些基于酶联免疫吸附测定(ELISA)的化学发光检测试剂盒具有出色的信号与噪声比。
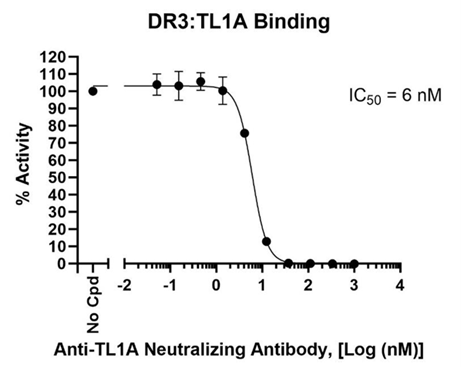
图3. 抗TL1A中和抗体(cat#101729)对DR3:TL1A结合的剂量依赖性抑制作用(cat#82241)。
该细胞系(cat#78811)是一种受 TL1A 控制的 DR3/NF-κB 荧光素酶报告基因 Jurkat 细胞系,该细胞系能够表达萤火虫荧光素酶,并且其 NF-κB 反应元件的表达是稳定的,能够表达人DR3。萤火虫荧光素酶报告基因的表达由位于最小TATA启动子上游的NF-κB反应元件驱动。通过测量荧光素酶活性,可以监测由 DR3配体TL1A激活的 NF-κB 信号通路。这种稳定的细胞系非常适合用于测试和验证TL1A或DR3 的阻断剂,或者用于研究 DR3 细胞信号传导。该细胞系已被证实对 TL1A 和 TNF-α 刺激有反应。重组蛋白TL1A(cat#101880)的刺激被抗 TL1A 中和抗体(cat#101729)和 DcR3所阻断。
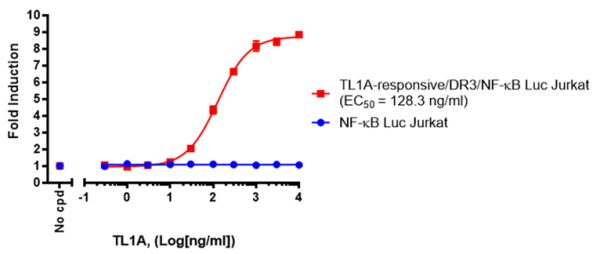
图4.在对TL1A反应型荧光素酶报告基因Jurkat细胞系中,TL1A的剂量反应情况与一个不表达DR3的阴性对照细胞系进行了比较
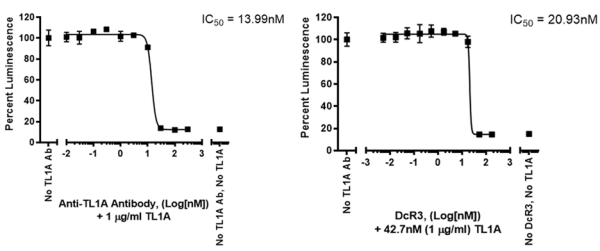
图5.抗TL1A抗体和DcR3 Fc融合蛋白对TL1A反应型荧光素酶报告细胞系Jurkat中 TL1A反应的抑制作用

微信扫码在线客服