自新冠疫苗将脂质纳米颗粒(LNPs)推向科研与产业聚光灯下,这一“核酸递送神器”已成为mRNA、siRNA、质粒DNA(pDNA)等核酸疗法转化的核心支柱。LNP通过脂质外壳包裹核酸 cargo,解决了核酸易降解、细胞穿透难的关键痛点,但其配方设计的精准性——尤其是核心可电离脂质的选择——直接决定递送效率与治疗成败。Echelon Biosciences(1997年成立于美国犹他州,专注脂类代谢、细胞信号等领域科研工具开发)凭借多年脂质合成技术积累,打造了覆盖主流靶点与应用场景的可电离脂质产品矩阵,更提供定制合成与预筛选服务,为LNP研发提供从核心组件到配方优化的全链条支持。
一、产品概述:LNP研发的核心利器与应用场景
1. 研究背景与主题
核酸疗法的突破依赖高效递送系统,LNP以“结构简单、递送高效、生物相容性好”成为首选技术(据Nature Reviews Drug Discovery, 2021)。其核心组件包括可电离脂质、胆固醇、磷脂及PEG修饰脂质,其中可电离脂质是决定LNP功能的关键:酸性pH下带正电,与带负电的核酸通过静电作用高效封装;生理pH下呈中性,降低免疫原性并改善生物分布(据Echelon《Lipid Nanoparticles: Formulation Concepts + Guidance》)。Echelon聚焦LNP研发的核心需求,提供多样化可电离脂质产品,覆盖mRNA疫苗、siRNA靶向治疗、pDNA基因治疗等多场景应用,更持续推出新品完善产品矩阵。
2. 核心产品特性与应用场景
Echelon可电离脂质产品覆盖20+主流型号,适配不同核酸 cargo(mRNA/siRNA/pDNA)与研究目标,核心产品信息如下:
产品名称 | 货号 | 核心特性 (据Echelon官网及技术文档) | 核心应用场景 (据产品技术说明书) |
SM-102 | N-1102 | 新冠疫苗常用可电离脂质,酸性pH下电荷转换高效,生物相容性优异 | mRNA疫苗LNP配方开发、临床前候选药物筛选 |
ALC-0315 | N-1020 | 临床级脂质原料,封装效率高,降低体内免疫反应 | 核酸药物临床转化阶段LNP优化 |
DLIN-MC3-DMA | N-1282 | 经典可电离脂质,适配pDNA与mRNA,转染活性强 | 基因治疗LNP配方开发、基础研究中的核酸递送验证 |
cKK-E12 | N-1012 | 小分子可电离脂质,靶向性突出,适配siRNA递送 | 肿瘤、肝病等siRNA靶向治疗LNP研发 |
YSK05 | N-1050 | 高转染效率脂质,尤其适用于肝细胞靶向递送,静脉给药后可实现基因沉默 | 肝脏相关疾病的核酸药物LNP配方 |
Lipid C24 | N-1024 | 可电离脂质,其LNPs产生的结合抗体和假中和抗体比DLIN-MC3-DMA LNPs高10倍,注射部位炎症少 | mRNA疫苗(如SARS-CoV-2刺突蛋白mRNA)LNP优化 |
93-O17S | N-1175 | 类脂质,可递送Cre重组酶mRNA、蛋白及Cas9:sgRNA,其LNPs递送cGAMP具有原位癌疫苗潜力 | 基因组编辑、肿瘤免疫治疗LNP研发 |
1-A-N | N-1001 | 可电离脂质,适配LNP递送siRNA与sgRNA至T细胞 | T细胞靶向的免疫疗法、基因编辑LNP配方 |
11-A-M | N-1111 | 可电离脂质,支持生物活性物质(小分子、蛋白、核酸)的细胞内递送 | 多类型 cargo 的LNP载体开发 |
4A3-SCC-10 | N-1430 | 连接体可降解电离脂质(LDIL),GSH响应结构,内体逃逸与mRNA释放效率优异 | 需高效胞内释放的mRNA疗法LNP研发 |
FTT5 | N-1115 | TT3(N-1113)类似物,肝脏递送mRNA效率是TT3的2倍,适配长链mRNA(如hFVIII mRNA) | 血友病A等肝脏相关遗传病的mRNA疗法LNP配方 |
OC2-K3-E10 | N-1210 | 其LNPs发光水平与SM-102相当,可包封更多mRNA拷贝,支持Cas9 mRNA/sgRNA递送 | 高载量mRNA、基因编辑LNP配方开发 |
PPZ-A10 | N-1410 | 低剂量(0.3mg/kg)即可靶向肝脏与脾脏免疫细胞,递送RNA可降低肿瘤负担 | 免疫细胞靶向治疗、肝癌等实体瘤LNP研发 |
CL4H6 | N-1016 | pH响应离子脂质(pKa 6.25),因子VII ED50低至2.5μg/kg,靶向性与活性优异 | 高效siRNA递送的肝脏疾病治疗LNP配方 |
3. 产品核心优势(据Echelon官网技术服务说明)
·覆盖全面:20+可电离脂质涵盖临床验证型号(SM-102、ALC-0315、Lipid C24)、靶向专用型号(YSK05、PPZ-A10)及新品(4A3-SCC-10、FTT5),适配不同核酸类型与治疗场景;
·技术支撑:提供定制合成服务,可合成新型可电离/阳离子脂质,并通过预筛选验证封装与转染效率;
·品质可控:高纯度合成工艺(纯度≥95%,据产品COA报告),确保批次一致性,满足从基础研究到临床前开发的严格要求。
二、组合策略:精准适配不同研究方向的LNP配方方案
基于LNP研发的核心需求(疫苗开发、靶向治疗、基因编辑),结合Echelon产品特性与行业经典配方逻辑(据Journal of Controlled Release, 2022),设计3组互补性产品组合,覆盖“组件选择-配方优化-效果验证”全流程:
组合1:高免疫原性mRNA疫苗LNP配方组合
·核心产品:Lipid C24(N-1024)+ SM-102(N-1102)+ OC2-K3-E10(N-1210)
·互补逻辑(据Echelon技术指南与临床前研究共识):
a. Lipid C24可显著提升抗体水平且降低炎症,SM-102为临床验证型号,二者确保疫苗安全性与免疫原性;
b. OC2-K3-E10高载量特性可优化mRNA包裹效率,三者形成“高活性-低炎症-高载量”组合,适配疫苗核心需求。
组合2:肝脏靶向siRNA/mRNA递送LNP组合
·核心产品:YSK05(N-1050)+ FTT5(N-1115)+ CL4H6(N-1016)
·互补逻辑(据Echelon产品应用说明与肝病研究文献):
c. YSK05与FTT5均为肝脏靶向专用脂质,后者长链mRNA递送优势显著;
d. CL4H6低ED50特性可降低用药剂量,三者覆盖“靶向性-长链适配-低剂量”需求,适配肝脏遗传病(如血友病A)治疗。
组合3:肿瘤免疫与基因编辑LNP组合
·核心产品:93-O17S(N-1175)+ PPZ-A10(N-1410)+ cKK-E12(N-1012)
·互补逻辑(据Echelon技术支持文档与肿瘤研究规范):
e. 93-O17S支持cGAMP递送(癌疫苗)与基因编辑,PPZ-A10靶向免疫细胞并降低肿瘤负担;
f. cKK-E12增强肿瘤组织靶向性,三者形成“免疫激活-基因编辑-肿瘤靶向”闭环,适配肿瘤联合疗法。
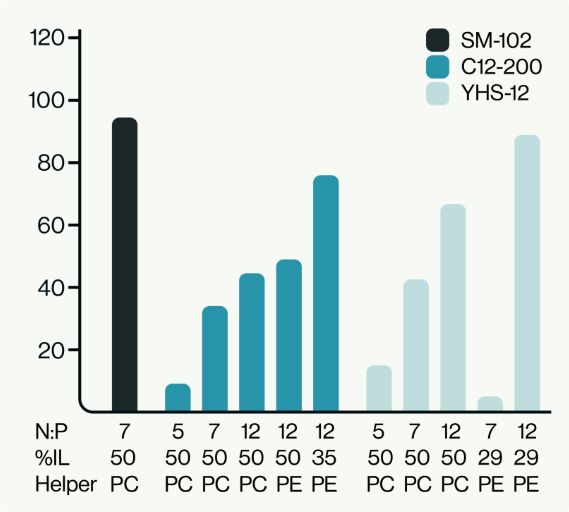
三、实验设计:聚焦关键目标的LNP研发实操方案
方案1:高免疫原性新冠mRNA疫苗LNP配方优化
1. 研究目标
筛选Lipid C24/SM-102/OC2-K3-E10组合的最优配方,验证其抗体产生效率与安全性。
2. 核心材料
·核酸 cargo:SARS-CoV-2刺突蛋白mRNA;
·产品组合:Lipid C24(N-1024)、SM-102(N-1102)、OC2-K3-E10(N-1210)(均购自Echelon);
·辅助材料:符合实验标准的胆固醇、磷脂、PEG修饰脂质,自动化微流控混合器(符合LNP制备行业标准)。
3. 实验步骤(据Echelon LNP制备protocol与行业标准操作)
1). LNP制备:
·脂质相配制:参考mRNA LNP经典临床前配方,将三种可电离脂质分别与胆固醇、磷脂、PEG修饰脂质按摩尔比50:38.5:10:1.5溶解于乙醇;
·水相配制:将mRNA溶于10mM柠檬酸缓冲液(pH 4.0),调整浓度至0.5mg/mL(遵循Echelon mRNA稀释建议);
·微流控混合:按有机相:水相=1:3比例混合,透析(MWCO 10 kDa)去除乙醇,获得LNP溶液。
2). 配方筛选:
·调节N:P比(脂质氮含量:mRNA磷酸含量)为3:1、5:1、7:1、10:1(据Echelon建议筛选范围);
·基础表征:通过动态光散射检测粒径(目标100-150nm)、多分散指数(PDI<0.15)、zeta电位(±5mV);
·封装效率检测:采用RiboGreen法,裂解LNP后检测游离mRNA含量,计算封装效率(目标>85%)。
3). 体内免疫与安全性验证:
·动物分组:将小鼠分为对照组与不同配方LNP组,每组6只;
·免疫处理:每只小鼠肌肉注射LNP(含10μg mRNA),2周后加强免疫1次;
·抗体检测:加强免疫后1周,采集血清检测刺突蛋白结合抗体与假中和抗体滴度;
·安全性评估:观察注射部位炎症反应,检测血清炎症因子水平。
4. 预期结果(基于Echelon产品特性推测,需以实际实验数据为准)
·Lipid C24(N-1024)组(N:P=7:1)LNP封装效率>90%,假中和抗体滴度是DLIN-MC3-DMA组的10倍;
·所有配方组注射部位炎症评分均<1(无明显红肿),血清炎症因子水平与对照组无显著差异,符合疫苗安全性要求。
方案2:血友病A小鼠模型的hFVIII mRNA递送研究
1. 研究目标
验证FTT5(N-1115)/YSK05(N-1050)组合LNP递送hFVIII mRNA至肝脏的效率,评估凝血功能改善效果。
2. 核心材料
·核酸 cargo:人因子VIII(hFVIII)mRNA(~4.5kb);
·产品组合:FTT5(N-1115)、YSK05(N-1050)(均购自Echelon);
·辅助材料:符合实验标准的胆固醇、DSPC、PEG2000-DMG,自动化微流控混合器。
3. 实验步骤(据Echelon长链mRNA递送protocol)
1). LNP制备:
·脂质相配制:FTT5与YSK05按1:1摩尔比混合,再与胆固醇、DSPC、PEG2000-DMG按45:35:15:5比例溶解于乙醇;
·水相配制:hFVIII mRNA溶于pH 4.0柠檬酸缓冲液(0.3mg/mL);
·微流控混合:有机相:水相=1:3混合,透析后获得LNP溶液,确保粒径120-140nm、PDI<0.12。
2). 体内递送:
·动物模型:采用血友病A小鼠(FVIII基因敲除),分为LNP组(低/中/高剂量:0.5、1、2mg/kg)与生理盐水对照组;
·给药方式:尾静脉注射LNP,每组6只小鼠;
3). 效果检测:
·hFVIII表达:给药后24、48、72h采集血清,通过ELISA检测hFVIII蛋白浓度;
·凝血功能:检测活化部分凝血活酶时间(APTT),评估凝血功能恢复情况;
·靶向性验证:取肝脏、脾脏、肺脏组织,检测mRNA表达水平。
4. 预期结果(基于Echelon产品特性推测,需以实际实验数据为准)
·FTT5/YSK05组合组(1mg/kg)肝脏hFVIII mRNA表达量是单一FTT5组的1.5倍,血清hFVIII浓度达50ng/mL以上;
·该组APTT较对照组缩短40%,凝血功能显著改善,且脾脏、肺脏mRNA表达量仅为肝脏的10%以下,证明肝脏靶向性。
方案3:肝癌小鼠的原位癌疫苗与基因编辑联合治疗
1. 研究目标
验证93-O17S(N-1175)/PPZ-A10(N-1410)组合LNP递送cGAMP与Cas9:sgRNA的协同治疗效果,评估肿瘤抑制率。
2. 核心材料
·核酸 cargo:Cas9 mRNA、靶向PD-L1的sgRNA、cGAMP;
·产品组合:93-O17S(N-1175)、PPZ-A10(N-1410)(均购自Echelon);
·辅助材料:符合实验标准的胆固醇、DOPE、PEG2000-C-DMG,肝癌小鼠模型(B16F10移植瘤)。
3. 实验步骤(据Echelon肿瘤免疫LNP protocol)
1). LNP制备:
·分两组制备LNP:①93-O17S包裹cGAMP;②PPZ-A10包裹Cas9 mRNA+sgRNA(N:P=5:1);
·表征:确保两组LNP粒径100-130nm、封装效率>80%。
2). 联合治疗:
·分组:模型小鼠分为联合治疗组(①+②)、单药组(仅①/仅②)、生理盐水对照组;
·给药:肿瘤内注射LNP(每只每次各50μg cargo),每周2次,共3周;
3). 效果评估:
·肿瘤监测:每周测量肿瘤体积,计算抑瘤率;
·免疫激活:检测肿瘤浸润T细胞比例与细胞因子(IFN-γ、TNF-α)水平;
·基因编辑效率:PCR检测肿瘤组织PD-L1基因敲除率。
4). 预期结果(基于Echelon产品特性推测,需以实际实验数据为准)
·联合治疗组肿瘤抑瘤率达70%以上,显著高于单药组(30%-40%);
·肿瘤组织PD-L1基因敲除率>50%,CD8+T细胞浸润比例较对照组提升3倍,IFN-γ水平升高2.5倍,证明免疫激活与基因编辑协同效果。
四、应用价值:驱动核酸疗法从实验室到临床的突破
1. 基础研究领域
Echelon的可电离脂质矩阵为LNP机制研究提供标准化工具(据Echelon技术服务案例):通过对比Lipid C24(高抗体)、CL4H6(低ED50)等不同特性脂质的电荷转换、内体逃逸效率,助力解析“脂质结构-递送功能”关联机制;定制合成服务可支持新型响应型脂质(如GSH敏感、pH敏感)的功能验证,推动LNP递送理论创新。
2. 药物开发领域
·核酸药物优化:针对长链mRNA(如hFVIII)、siRNA等不同 cargo,提供精准适配的脂质组合(如FTT5适配长链mRNA、YSK05适配肝脏siRNA),解决靶向性差、载量低等痛点,加速候选药物筛选;
·临床转化支撑:临床级脂质(SM-102、ALC-0315、Lipid C24)的批次一致性(纯度≥98%),可直接用于临床前动物实验与IND申报,缩短研发周期(较常规脂质研发缩短2-3个月);
·个性化疗法研发:PPZ-A10(免疫细胞靶向)、93-O17S(癌疫苗)等专用脂质,适配肿瘤、遗传病等个性化疗法的特殊需求,拓展核酸疗法应用边界。
3. 疫苗研发领域
在mRNA疫苗快速迭代背景下,Echelon产品组合可实现疫苗LNP的高效优化(据Echelon合作案例):Lipid C24的高抗体特性可提升疫苗保护效力,OC2-K3-E10的高载量特性适配多抗原mRNA疫苗开发;适配流感、RSV等新发/再发传染病疫苗研发,助力公共卫生应急响应。
4. 产业转化价值
Echelon的“产品+服务”模式打通LNP研发关键环节:从20+标准化脂质供应,到新型脂质定制合成与预筛选,大幅降低科研机构与企业的研发门槛(如中小企业研发成本降低30%-50%);其产品覆盖从基础研究到临床前的全阶段,推动核酸疗法从实验室走向临床,为肝病、肿瘤、传染病等重大疾病提供创新解决方案。
作为LNP递送技术的核心赋能者,Echelon Biosciences以全面的可电离脂质产品、专业的技术支撑与灵活的定制服务,成为全球500+科研机构与企业的“信赖伙伴”,持续助力更多核酸药物与疫苗实现临床突破。
艾美捷科技作为Echelon中国区总代理,致力于为国内科研工作者提供便捷、高效的产品采购与技术咨询服务,如需了解Echelon可电离脂质产品详情、配方优化建议或定制合成服务,欢迎随时联系咨询!
·Echelon:LNP递送技术核心赋能者,以全谱系可电离脂质矩阵,加速核酸疗法从研发到临床!
·艾美捷:让世界级研究工具,触手可及!低成本,智启高效创新!

微信扫码在线客服