在癌症免疫疗法领域,免疫检查点阻断疗法(Checkpoint Blockade Therapy)已成为一种具有显著临床效益的治疗手段,尤其是对于多种恶性肿瘤患者。该疗法通过靶向细胞毒性T淋巴细胞相关抗原-4(CTLA-4)和程序性死亡受体-1(PD-1)等免疫调节受体,能够重新激活被肿瘤诱导的免疫抑制所抑制的T细胞,从而实现对肿瘤的有效控制。然而,关于这类疗法所激活的T细胞所针对的肿瘤抗原的具体身份,以及这些抗原是否能被用于开发高度肿瘤特异性的疫苗,目前尚知之甚少。

在一项研究中,华盛顿大学的研究人员在《Nature》杂志上发表了名为“ Checkpoint Blockade Cancer Immunotherapy Targets TumourSpecific Mutant Antigens”的文章。文章旨在通过基因组学和生物信息学方法,鉴定在接受αPD-1和/或αCTLA-4治疗的、携带进行性生长肉瘤的小鼠模型中,肿瘤特异性突变抗原(TSMA)作为T细胞排斥抗原的角色。研究进一步探索了基于这些突变表位的合成长肽(SLP)疫苗,在诱导肿瘤排斥方面的效果,以及其与检查点阻断免疫疗法的比较。
研究方法
1. 实验模型与肿瘤移植
实验模型:研究使用了两种不同的进行性MCA肉瘤细胞系(d42m1-T3和F244),并将这些细胞系移植到野生型(WT)小鼠体内。
治疗与评估:小鼠接受αPD-1和/或αCTLA-4的治疗,并评估肿瘤的生长和排斥情况。通过注射耗竭CD4+或CD8+细胞的抗体或中和IFN-γ的抗体来确认免疫排斥的机制。
2. MHC I类表位预测
基因突变分析:通过cDNA捕获测序鉴定d42m1-T3细胞系中的非同义突变,并将这些突变转化为相应的蛋白质序列。
表位预测算法:使用三种MHC I类表位结合算法(稳定矩阵法、人工神经网络算法和NetMHCpan算法)预测表位加工和结合亲和力,计算每个预测表位的中位结合亲和力。表位筛选:应用过滤条件,包括去除预测加工不良的表位、来自假设蛋白的表位以及与其对应野生型序列相比结合亲和力较低的表位。
3. 肿瘤浸润淋巴细胞(TILs)的分析
四聚体染色:使用加载有预测突变表位的H-2K^b或H-2D^b四聚体染色新鲜分离的CD8+ TILs,以鉴定特异性T细胞。
细胞因子检测:通过ELISPOT和细胞内细胞因子染色检测IFN-γ和TNF-α的产生,以评估T细胞的活性。
4. 疫苗实验
疫苗制备:合成包含突变表位的长肽(SLP),并与聚肌胞苷酸(poly I:C)一起作为疫苗。
疫苗接种:将疫苗注射到已建立肿瘤的小鼠体内,评估肿瘤排斥和生存情况。
5. RNA测序与基因表达分析
RNA提取与测序:从经过不同检查点阻断治疗的小鼠的mLama4特异性CD8+ TILs中提取RNA,并进行RNA测序。
基因表达分析:使用DESeq2 R包分析差异表达的基因,并进行基因集富集分析(GSEA),以揭示不同治疗途径中受调节的通路。
研究结果
1. 检查点阻断免疫治疗诱导肿瘤排斥
肿瘤排斥:d42m1-T3和F244肉瘤细胞系在接受αPD-1和/或αCTLA-4治疗的野生型小鼠体内被排斥。排斥是免疫性的,因为它可以通过耗竭CD4+或CD8+细胞或中和IFN-γ来消除,并且在缺乏T、B和NKT细胞的Rag2-/-小鼠或缺乏CD8α+/CD103+树突状细胞的Batf3-/-小鼠中不发生。
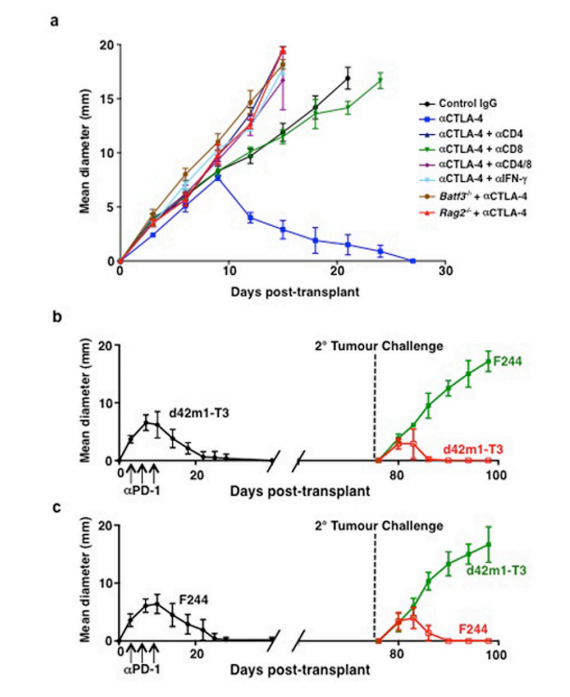
免疫检查点阻断治疗后,d42m1-T3的排斥需要先天和适应性免疫组分的参与:a. Rag2?/?、Batf3?/?或野生型小鼠队列分别接受对照单克隆抗体(mAb)、αCD4、αCD8α或αIFN-γ单克隆抗体处理,随后皮下注射1×106个d42m1-T3肿瘤细胞,并在移植后第3、6和9天接受αCTLA-4治疗。b、c. d42m1-T3(b)或F244(c)肿瘤细胞皮下注射到野生型小鼠(n=5)中,随后在移植后第3、6和9天接受αPD-1治疗。在肿瘤被排斥50天后,小鼠再次接受d42m1-T3或F244肿瘤细胞的挑战。
2. 突变表位鉴定
表位预测与验证:通过生物信息学方法预测了d42m1-T3细胞系中多个潜在的MHC I类结合表位,并通过四聚体染色和细胞因子检测验证了其中两个主要的表位:mLama4和mAlg8。
质谱验证:使用发现质谱(MS)和靶向选择反应监测(SRM)MS方法在d42m1-T3肿瘤细胞的H-2K^b洗脱物中检测到了mLama4和mAlg8表位。
3. 疫苗的有效性
肿瘤排斥与生存:与接受无关HPV长肽疫苗或仅接受poly I:C的小鼠相比,接种了包含mLama4和mAlg8表位的长肽疫苗的小鼠在建立肿瘤后显示出显著的肿瘤排斥和生存益处。
预防性疫苗接种:预防性接种mLama4和mAlg8长肽疫苗的小鼠在接种肿瘤细胞后显示出更高的生存率。
4. 基因表达与通路分析
基因表达变化:不同检查点阻断治疗对mLama4特异性CD8+ TILs的基因表达产生了大多治疗特异性的改变,涉及CD8+ T细胞效应功能的不同基因集。
通路分析:GSEA揭示了不同治疗途径中受调节的通路,包括效应功能、MAPK、趋化因子和细胞因子受体信号通路以及代谢和IL-2信号通路等。
5. 功能表型的变化
制性受体表达:经过αPD-1和/或αCTLA-4治疗的小鼠的mLama4或mAlg8特异性CD8+ TILs显示出较低的淋巴细胞激活基因3(LAG-3)和T细胞免疫球蛋白和粘蛋白蛋白3(TIM-3)表达。
细胞因子产生:治疗后的TILs显示出增强的IFN-γ和TNF-α产生,特别是接受αCTLA-4或αCTLA-4+αPD-1组合治疗的小鼠。
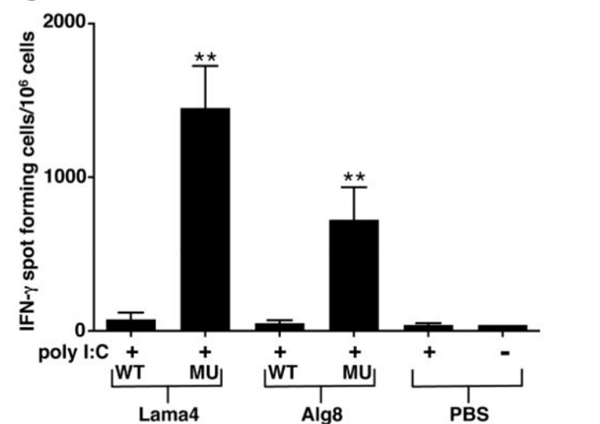
IFN-γ ELISPOT分析mLama4或malg8 SLP加polyI:C免疫小鼠的肽刺激脾细胞(每组n=3只小鼠)
在免疫检查点阻断研究期间,研究者多次使用mabtech IFN-γ ELISpot检测来表征抗原特异性T细胞在接受抗CTLA-4治疗前后的功能。根据种属,板子类型,酶标物等因素的不同,mabtech可提供多种IFN-γ ELISpot试剂盒以满足不同客户的需求:
| 货号 | 名称 | 用途 |
| 3321-4APT-2 | ELISpot Plus: Mouse IFN-γ (ALP) | 用于通过ELISpot检测法计数分泌小鼠IFN-γ的细胞 |
| 3321-4APW-2 | ELISpot Plus: Mouse IFN-γ (ALP) | |
| 3321-4AST-2 | ELISpot Plus: Mouse IFN-γ (ALP) | |
| 3321-4HPT-2 | ELISpot Plus: Mouse IFN-γ (HRP) | |
| 3321-4HPW-2 | ELISpot Plus: Mouse IFN-γ (HRP) | |
| 3321-4HST-2 | ELISpot Plus: Mouse IFN-γ (HRP) | |
| 3420-2APT-2 | ELISpot Pro: Human IFN-γ (ALP) | 用于通过ELISpot检测法计数分泌人IFN-γ的细胞 |
| 3420-2APW-2 | ELISpot Pro: Human IFN-γ (ALP) | |
| 3420-2AST-2 | ELISpot Pro: Human IFN-γ (ALP) | |
| 3420-2HPT-2 | ELISpot Pro: Human IFN-γ (HRP) | |
| 3420-2HPW-2 | ELISpot Pro: Human IFN-γ (HRP) | |
| 3420-2HST-2 | ELISpot Pro: Human IFN-γ (HRP) | |
| 3420-4APT-2 | ELISpot Plus: Human IFN-γ (ALP) | |
| 3420-4APW-2 | ELISpot Plus: Human IFN-γ (ALP) | |
| 3420-4AST-2 | ELISpot Plus: Human IFN-γ (ALP) | |
| 3420-4HPT-2 | ELISpot Plus: Human IFN-γ (HRP) | |
| 3420-4HPW-2 | ELISpot Plus: Human IFN-γ (HRP) | |
| 3420-4HST-2 | ELISpot Plus: Human IFN-γ (HRP) |
上一篇:Anaspec:Aβ肽

微信扫码在线客服